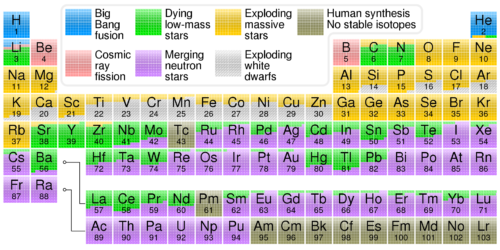
De nucleosynthese van de elementen. Dubbelklikken om de afbeelding te nucleosynthesiseren. Credit: CMglee/Wikipedia.
Nucleosynthese is het proces waarbij kernen van zwaardere elementen, bestaande uit protonen en neutronen, worden opgebouwd uit lichtere elementen. We kennen allemaal van onze scheikundelessen nog wel het periodiek systeem, waarin de elementen keurig gerangschikt staan. Wat je daarin echter niet terug ziet is de oorsprong van de elementen, door welk proces ze gevormd zijn. En dat is wat de afbeelding hierboven wel laat zien, de processen die voor ieder element hebben gezorgd. En dat zijn er zoals je kunt zien zes, de volgende zes processen van de nucleosynthese, waarbij opgemerkt dat nr. 2 twee processen bevat, die van de lichte en zware sterren:
- de oerknal nucleosynthese: dit is de vorming van de allerlichtste elementen tijdens de oerknal, waarmee 13,8 miljard jaar geleden het heelal ontstond. Het waren in de periode tussen 10 seconden en 20 minuten na de oerknal vooral waterstof en helium die ontstonden en een beetje deuterium en lithium.
- de stellaire nucleosynthese: deze vindt plaats in de kern van sterren, een proces dat begon toen pakweg 200 miljoen jaar na de oerknal de eerste sterren ontstonden en dat vandaag de dag nog steeds door gaat. Zoals je aan de afbeelding ziet wordt er onderscheid gemaakt tussen de vorming van elementen door kernfusie in lichte sterren (vooral via de proton-proton cyclus), zoals onze eigen zon, en in zware sterren (vooral via de koolstof-stikstofcyclus en het s-proces).
- de supernovae nucleosynthese: dit is de vorming van elementen tijdens de explosie van een supernova. In type Ia supernovae, veroorzaakt door exploderende witte dwergsterren die te zwaar zijn geworden, kan op deze wijze magnesium tot en met nikkel ontstaan, in type II supernovae, zeer zware sterren die na de ijzerverbranding exploderen, kunnen nog zwaardere elementen vormen, met name door het zogeheten R-proces, waarbij heel snel (de R komt van ‘rapid’) neutronen worden ingevangen.
- Nucleosynthese door splijting van kosmische straling: hierbij worden elementen gevormd als zeer energierijke deeltjes van de kosmische straling andere deeltjes raken, zoals in de aardse atmosfeer of in de interstellaire ruimte met gas- en stofwolken gebeurt. Het zijn met name lichte elementen die zo kunnen ontstaan, zoals lithium, beryllium en boor.
- De articifiële nucleosynthese: ook de mens maakt elementen en wel in het laboratorium. Het betreft allemaal kortlevende, zeer zware elementen, die (vermoedelijk) niet in de vrije natuur voorkomen.
Bron: Wikipedia + Starts with a Bang.
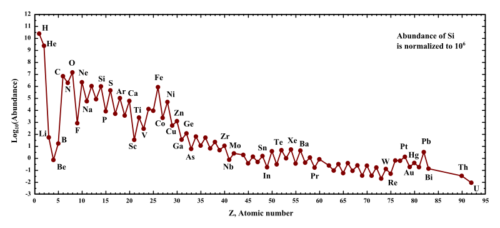





Ik vraag me af of de meeste Helium(He) op aarde wel afkomstig is van de Big Bang, of van alfa-verval van radioactieve elementen…
(Als ik me niet vergis, lekt He continu weg vanuit de atmosfeer de ruimte in. Zonder aanvulling uit radioactieve bron, was er niks meer in de atmosfeer.)
Kennelijk is het diagram gebaseerd op aardse elementen, anders zou er bij ‘groep 5’ niet staan :
” die (vermoedelijk) niet in de vrije natuur voorkomen ”
Na een supernova zullen deze elementen ook heus wel ontstaan (vermoedelijk), maar zijn door hun korte halfwaardetijd NU niet meer te vinden op Aarde ( en ons zonnestelsel).
Groet, Paul
Helium komt niet alleen in de atmosfeer voor. Aanvulling van Helium in de atmosfeer komt uit de aarde zelf (gesteente en oceaanwater).
Globaal bestaat ons zonnestelsel voor 99% uit H en He. De Zon bezit zo’n 99% van alle aanwezige materie/massa, en van de leftovers heeft Jupiter zo’n 99% ingepikt.
Uiteraard is het gebaseerd op aardse elementen, of eigenlijk zonnestelsel-elementen. Zonnestelsel, omdat meteorieten van het type chondrites voornamelijk zijn gebruikt om de samenstelling van ons zonnestelsel vast te stellen. Ruwweg kan je stellen dat ons diagram een afspiegeling is van de elementen (soort en hoeveelheid) zoals die te vinden zijn in “zonnestelsels” die zo’n 9 miljard jaar geleden zijn gevormd. Een ouder zonnestelsel zal over minder zware elementen beschikken, een jonger stelsel over meer. Dus het diagram van een alien uit een stelsel van 10 miljard jaar oud zal zeker een andere verdeling laten zien, en misschien zelfs eerder stoppen en niet bij uranium zoals in de onze.
Dit blog is eigenlijk niet compleet wat verwarring kan geven…..maar ik klikte op het trefwoord “nucleosynthese” en vond nog een paar goede blogs over dit onderwerp; http://www.astroblogs.nl/tag/nucleosynthese/
Eigenlijk “moet” je ze allemaal even doorspitten om een completer beeld te krijgen.
Paul, dat zeldzame helium op aarde is vermoedelijk grotendeels ontstaan door radioactief verval, wat je dus ook noemt, en niet van de oerknal. Het is vooral het verval van thorium en uranium dat helium produceert.
Alhoewel heel het heelal vol zit met Helium, hebben het er op Aarde maar verdomd weinig van.
Schijnbaar heeft men niet door hoe weinig, want elk jaar weer word het verspild
om o.a. feestjes op te vrolijken, door het in ballonnen te stoppen, omdat die dan zo leuk omhoog gaan.
En zo zijn er nog wel honderden van verspilling te noemen. Nadeel is dat het goedkoper is dan
wat men hier in Nederland per liter voor benzine betaald, dat werkt verspilling in de hand.
En als iets op een gegeven moment op is, kan je het niet meer toepassen, dan begint het gedonder pas goed.
En dan heb ik het alleen nog maar over Helium…
Maar goed, laat ik geen doemdenker worden, en er van uit gaan dat de wijsheid ooit de mens zal treffen 🙂
Je hebt grotendeels gelijk.
In een ster is hoofdzakelijk sprake van “gewone” fusie. Samenpersen van nucleus om zwaardere elementen te maken. Inderdaad ligt de grens bij ijzer omdat dit element de grootste bindingsenergie heeft. De fusie (simpel gezegd de hitte) zorgt ervoor dat de ster niet instort vanwege de zwaartekracht. Het is een proces dat zichzelf in stand kan houden zolang er brandstof is. Hoe zwaarder de ster, hoe groter de druk/temperatuur in/nabij de kern, hoe zwaarder de elementen die het kan maken. Voor onze zon is de koek op zodra alle beschikbare H omgezet in He
Maar het proces tijdens een nova is anders. Hier ontstaan de zwaardere elementen door het invangen van neutronen. Tijdens de nova is er een enorme energie en enorme hoeveelheid vrije neutronen. Door die enorme energie ondergaan de nucleus/atomen een bombardement van neutronen en zullen er ook invangen. Door de enorme snelheid van het hele gebeuren, ontstaat er ook een brug over het gat van onstabiele elementen/isotopen. 1 extra neutron kan tot een onstabiele nucleus leiden, maar omdat het snel een 2e neutron voor zijn kiezen krijgt, onstaat er een nieuwe nucleus dat wel stabiel is (nog voordat de onstabiele nucleus kan vervallen). Een nova is ook een korte gebeurtenis en niet een proces dat zichzelf in stand kan houden….het mag dus energie kosten, met zwaardere elementen als een gevolg.
Ps, het aantal protonen bepalen het atoomtype. Het aantal protonen is gelijk aan de electronen. Neutronen veranderen niet het atoom maar voegen massa toe. Een atoom met meer neutronen dan protonen noemt men een isotoop. Neutronen zijn wel belangrijk. De protonen hebben een electromagnetische lading en ze zouden zichzelf af moeten stoten en geen atoomkern kunnen vormen. De bindingsenergie is de nucleaire kracht. Neutronen voegen nucleaire kracht toe, zonder electromagnetische kracht toe te voegen, ze zijn immers electromagnetisch-neutraal. Met als resultaat dat de nucleaire kracht de electromagnetische kan overwinnen….
Tja….en toen was de vraag verdwenen waarop ik bovenstaande reply tikte 🙁
post deleted?
Huh, is er iets verdwenen? Ik zie niets in het spamfilter staan hoor. ❓
Inderdaad….er stond een redelijk lange post….de vraag was in grote lijnen, hoe het kan dat er zwaardere elementen in een nova gemaakt kunnen worden, ondanks dat het proces energie kost. Die post stond ook op de hoofdpagina in verkorte vorm (balkje rechts). Ik ben de naam vergeten maar het was geen geregistreerde gebruiker.
Zouden er – in theorie – als het universum nog veel ouder wordt, laten we zeggen over 10 miljard jaar, processen mogelijk zijn waarbij nog zwaardere, nu nog niet bekende elementen worden gevormd?
En nog een andere vraag: is op basis van het atoomgetal enige voorspelling mogelijk aangaande de stabiliteit van elementen? M.a.w.: al die door mensen gemaakte elementen zijn niet stabiel, maar zou het mogelijk zijn dat er op een gegeven moment wél een stabiel element wordt gemaakt en zo ja, is er dan iets te zeggen over de eigenschappen van dat element?
groet,
Gert (Enceladus)
Zover ik weet heeft Uranium-238 het maximaal mogelijke aantal protonen en neutronen die je in een atoomkern kan proppen. Zwaardere elementen zou niet mogelijk zijn. (238 is het aantal protonen en neutronen samen)
Weer zover ik weet 🙂 een onstabiel element kan een stabiele zwaardere isotoop worden door er 1 of meer neutronen aan toe te voegen. Dat isotoop is hetzelfde element maar met iets meer massa. Ik weet niet of dit zomaar op kan gaan voor de man-made elementen, heb ik me nog nooit in verdiept.
(In ons zonnestelsel zou je 80 elementen kunnen vinden met 339 isotopen)
Negentig (!) elementen.
Paul
Je hebt helemaal gelijk……80 is het aantal stabiele elementen (dus niet onderhavig aan radioactief verval) en niet het totaal van de van nature voorkomende elementen.
Excuse moi 🙂
Vraag 1)
Nee !
In zware sterren die uiteindelijk een Zwart Gat vormen, is de druk/temperatuur al zo hoog
dat alles daar mogelijk zou zijn.
Over 10 of 100 miljard jaar zijn die processen echt niet anders. 13 mjd. jaar geleden, vlak na de BB, was het ook al niet anders dan nu ! [ Ook toen waren er al Supernovae. ]
Als er nog zwaardere stabiele elementen mogelijk zijn, is het ook mogelijk dat er NU al ergens wat van deze elementen zijn. Misschien wel op Aarde, maar we hebben ze nooit gevonden.
De kans is ook niet erg groot, omdat Supernovae zeer snel verlopen, en er dus weinig tijd is om deze stabiele elementen te vormen.
Vraag 2)
Op Aarde kunnen we gunstige omstandigheden misschien veel langer vast houden, zodat de kans op vorming van dergelijke stabiele elementen groter wordt. Maar ik weet niet óf er überhaupt nog stabiele elementen zijn. Men vermoedt van wel…. zekerweten doen we nog niet.
Misschien dat we nog beter inzicht krijgen in de neutron-bindingsenergie, zoals K.J. hier boven beschrijft. Met deze verbeterde inzicht kunnen we wellicht voorspellen welke ‘configuraties’ wel een stabiel geheel vormen.
Eigenschappen?
– Het zal een metaal zijn. Alle zwaardere elementen zijn een metaal.
– { en het is vast rood, omdat ik dat een mooie kleur vind. 😛 }
Groet, Paul
Er zijn ongeveer 92 natuurlijke elementen; natuurlijke elementen komen op de aarde voor. Er zijn nu ongeveer 15 kunstmatige elementen; kunstmatige elementen zijn elementen die gemaakt zijn in een laboratorium of tijdens kernsplijting in een kerncentrale ontstaan. Theoretisch kun je nog heel veel elementen erbij maken, maar praktisch is een ander verhaal.
http://www.megawetenschap.nl/elementen.html
En psst..ik ben allergisch voor #27 Kobalt (Co), #28 Nikkel (Ni) en Chromaat
http://upload.wikimedia.org/wikipedia/commons/9/98/Periodic_table_%28polyatomic%29.svg
@K.J.
Dat ijzer het laatste fusieprodukt is in sterren heeft te maken met dat ijzer het laatste stabiele element is wat in zijn fusieproces nog energie oplevert, elke fusie voor de zwaardere elementen gebruikt energie. Volgens mij, maar ik kan er naast zitten natuurlijk, heeft het niet te maken met dat ijzer de grootste bindingsenergie heeft.
En opzich is elk element een isotoop, niet alleen elementen die meer neutronen dan protonen hebben. Bijvoorbeeld helium-3, 2 protonen en 1 neutron, is ook gewoon een heliumisotoop.
Een isotoop van hetzelfde element is dan ook gewoon een atoom met een verschillend aantal neutronen.
http://nl.wikipedia.org/wiki/Isotoop
http://nl.wikipedia.org/wiki/Isotopentabel
En dat de zwaardere elementen in een nova gemaakt kunnen worden ondanks dat dit energie kost komt mijn inziens ook mede door de implosie van de supernova. Deze implosie drukt de deeltjes samen in nieuwe zwaardere elementen.
En uranium-238 is niet het zwaarste element, zie http://nl.wikipedia.org/wiki/Isotopentabel . Hierin heb je röntgenium-272 en darmstadtium-272.
En als ik naar de man-made atomen kijk heb je element 117 en 118 met atoomgetal 294, ununseptium-294 en ununoctium-294.
Naast de 80 bekende stabiele elementen zou er nog een island of stability kunnen zijn die stabiele zwaardere elementen voorspelt.
http://en.wikipedia.org/wiki/Island_of_stability
Of je met het toevoegen. of verwijderen, van neutronen altijd tot een stabiel element zal komen weet ik niet. Je zou haast denken van wel, maar ik denk dat er meer bij komt kijken, een soort verhouding protonen en neutronen en hun bindingsenergie.
Quote van Rudiev : “Of je met het toevoegen. of verwijderen, van neutronen altijd tot een stabiel element zal komen…”
…, blijkt uit de isotopen tabel. Het is NIET zo !!
bv Technetium (Atoom nr. 43) heeft geen enkele stabiele isotoop, Prometium (nr. 61) idem dito.
Ook van translood elementen (82+) zijn tot nu toe nog geen stabiele kernen bekend.
Misschien in het eerste of zelfs tweede ‘eiland van stabiliteit’ 😉
Groet, Paul
Wat, is er een twééde eiland van stabiliteit? Weer wat geleerd 😉
Genoeg over te googlen, bijvoorbeeld:
http://www.sciencedaily.com/releases/2008/04/080406114739.htm
Ja Olaf !
Ik wist het ook niet, maar volgens Wikipedia zou er nog een tweede eiland van stabiliteit kunnen zijn.
Zo rond atoomnummer 164 met een massa van 482. Dit alles natuurlijk nog slechts hypothetisch, maar dat is het eerste eiland ook.
Het geeft wel aan dat er kennelijk toch kennis/kunde is, anders doet men niet zo’n gericht voorspelling!
Groet, Paul
http://en.wikipedia.org/wiki/Island_of_stability
chagrijn!
🙂
😕
Rudiev, een paar dingen ga ik zo in mee, een paar niet.
Dat ijzer de meest stabiele kern heeft en hoogste bindingsenergie, heeft juist als gevolg dat er meer energie nodig is om het te fuseren dan er vrij zal komen. Tot ijzer zal bij fusie een deel van de aanwezige energie in de oorspronkelijke atomen vrij worden gegeven en zal het een evenredig deel aan massa verliezen. Na ijzer zal er door splitsing een deel van de aanwezige energie worden vrijgegeven en zal er wat massa verdwijnen. Ps, het is een misvatting dat hier eenvoudig sprake is van materie omzetten in energie (of energie in materie), wat E=MC2 wel doet vermoeden. Wat mij betreft is dat pittige stof. Hier kan je er wat over vinden
http://en.wikipedia.org/wiki/Mass%E2%80%93energy_equivalence
http://hyperphysics.phy-astr.gsu.edu/hbase/astro/nucsyn.html#c1
Elk element is een isotoop > ga ik zo in mee. Het is meer mijn voertaal om te spreken over elementen en diens variaties als isotopen.
Zwaardere elementen uit een nova > ga ik ook zo in mee. Het zal een combinatie zijn van fusie, fission en neutronen vangen zijn.
Zwaarste element > Ik denk dat we (misschien mijn schuld) natuurlijk voorkomende elementen in ons zonnestelsel, natuurlijk voorkomende elementen op aarde, stabiele natuurlijke elementen door elkaar gebruiken. Op aarde is naar mijn mening uranium-238 het zwaarste natuurlijk voorkomend element.
Dat island of stability > heb ik ooit iets over gelezen…volgens mij is het bestaan ervan amper meer dan een vaag vermoeden?
Het laatste stukje, ik zal er een keer wat over schrijven met een paar voorbeelden. Maar dat kan ik nu niet effe uit de mouw schudden 🙂
Btw, soms kom je onverwachts leuke dingen tegen op internet.
Dit was b.v. helemaal nieuw voor me en het zet Einstein wel een beetje op een andere trede op de ladder voor mijn gevoel; http://en.wikipedia.org/wiki/Nikolay_Umov
SNIP
He was the first scientist to indicate interrelation between mass and energy proposing the formula E=kmc2 with 0,5 =< k =< 1 as early as in 1873
/SNIP
En deze, ook wel een beetje opmerkelijk. Je kan t/m hoofdstuk 7 scrollen door simpel het getal in de url te wijzigen. Vooral hoofdstuk 2 is goed leesvoer.
http://mpbundels.mindef.nl/35_serie/35_310/hoofdstuk_1.htm